
探讨孕妇红细胞血型不规则抗体的分布及特点。
选择2016年1月至2018年6月,于青岛市中心血站进行红细胞血型不规则抗体鉴定的130例孕妇为研究对象。其年龄为25~42岁,中位年龄为32岁。对这130例孕妇的ABO及Rh血型进行鉴定,同时对其Rh血型系统不规则抗体效价采用试管法进行测定,红细胞血型不规则抗体筛查与鉴定采用微柱凝胶法或者试管法。本研究遵循的程序符合2013年修订版《世界医学协会赫尔辛基宣言》要求,并且与所有受试者签署临床研究知情同意书。
①纳入研究130例孕妇中,A、B、O、AB型血型为44例(33.8%)、48例(36.9%)、27例(20.8%)和11例(8.5%);Rh阳性为90例(69.2%),Rh阴性为40例(30.8%)。②本研究130例孕妇的血清标本中,Rh、MNSs、P、Lewis血型系统不规则抗体为71例(54.6%)、28例(21.5%)、3例(2.3%)和14例(10.8%),抗-HI为4例(3.1%)。③ 71例检出Rh血型系统不规则抗体的孕妇中,检出率最高的抗体效价为2,其检出率为26.8%(19/71)。抗体效价系512的孕妇为1例,其Rh血型为阴性,既往有RhD阳性红细胞制品输血史。
青岛市红细胞血型不规则抗体阳性孕妇的不规则抗体分布,以Rh血型系统为主,其次是MNSs血型系统。对孕妇进行产前红细胞血型不规则抗体筛查和鉴定,有利于保证孕妇输血安全,以及降低新生儿溶血病(HDN)的发生风险。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
随着现代临床输血技术的不断发展,ABO血型不合导致的输血反应发生率已显著降低,红细胞不规则抗体引起的免疫性溶血性输血反应成为临床输血关注的热点。红细胞不规则抗体是指抗-A和抗-B以外的红细胞血型抗体,是引起血型鉴定及交叉配血困难、新生儿溶血病(hemolytic disease of newborn,HDN),以及输血不良反应的主要原因[1]。妊娠和输血是产生同种免疫性抗体的最主要原因。对孕妇进行产前红细胞血型不规则抗体筛查,发现具有临床意义的红细胞血型不规则抗体,及早采取预防和治疗措施,从而有效降低HDN发生率及缓解疾病临床症状[2]。本研究通过分析130例孕妇于青岛市中心血站血型室进行红细胞血型不规则抗体筛查和鉴定的检测结果,旨在发现具有临床意义的红细胞血型不规则抗体,有效保证临床输血安全,避免HDN的发生。现将研究结果报道如下。
选择2016年1月至2018年6月,于青岛市中心血站血型室进行红细胞血型不规则抗体鉴定的130例孕妇为研究对象。研究对象的年龄为25~42岁,中位年龄为32岁;初次妊娠孕妇为25例,既往有孕、产史或流产史者为105例;既往有输血史者为3例。研究对象纳入标准:产前检查时,红细胞血型不规则抗体初筛结果呈阳性者。排出标准:非自愿参加本试验者。本研究遵循的程序符合2013年修订版《世界医学协会赫尔辛基宣言》要求,并且与所有受试者签署临床研究知情同意书。
抗-A、抗-B单克隆抗体(批号:20161015、20170102、20180101,上海血液生物医药有限责任公司);抗-D抗体(批号:20171811、上海血液生物医药有限责任公司,批号:8000227190、荷兰Sanquin公司,批号:517097、加拿大Dominion公司);ABO反定型红细胞(批号:20175338、20185310、20185323,上海血液生物医药有限责任公司)。不规则抗体筛选细胞(Ⅰ、Ⅱ、Ⅲ)(批号:06280331、06280371、06280391,瑞士DiaMed公司;批号:8000247236、8000244382、8000246495,荷兰Sanquin公司)。不规则抗体鉴定谱细胞(批号:8000247238、8000247939、8000248526,荷兰Sanquin公司)。ID-Centrifuge 12 SⅡ型离心机(瑞士DiaMed公司),ID-Incubator 37 SⅠ型孵育器(瑞士DiaMed公司),KA2200型台式离心机(日本KUBOTA公司)。
于本研究130例孕妇肘正中静脉收集外周血10 mL,其中5 mL加入无抗凝剂的试管,5 mL加入乙二胺四乙酸(ethylenediaminetetraacetic acid,EDTA)抗凝管中。待无抗凝剂试管中的全血自凝后,于1 000×g离心5 min分离血清,用于红细胞血型不规则抗体筛查与鉴定。EDTA抗凝管于1 000×g离心5 min分离红细胞,红细胞经生理盐水洗涤3次后,配制成终浓度为3%的红细胞悬液,用于血型鉴定。
本研究中,130例孕妇的ABO及Rh血型鉴定、Rh血型系统不规则抗体效价测定采用试管法,红细胞血型不规则抗体筛查与鉴定采用微柱凝胶法或者试管法。红细胞血型不规则抗体筛查结果判读:若抗体筛查Ⅰ、Ⅱ、Ⅲ反应柱(管)中≥1柱(管)出现凝集反应,则抗体筛查结果判定为阳性,表示该血清样本中检出不规则抗体;若抗体筛查Ⅰ、Ⅱ、Ⅲ反应柱(管)均未出现凝集反应,则抗体筛查结果判定为阴性,表示该血清样本中未检出不规则抗体。红细胞血型不规则抗体鉴定时,根据1~16号谱细胞反应结果及凝集强度,对照反应格局表确认相应抗体。本研究所有血型血清学检验的实验操作严格按照《全国临床检验操作规程》(第4版)[3],以及试剂及仪器说明书进行。
本研究130例孕妇的ABO血型鉴定结果显示,A、B、O、AB型血型孕妇分别为44例(33.8%)、48例(36.9%)、27例(20.8%)和11例(8.5%)。Rh血型鉴定结果显示,Rh阳性血型孕妇为90例(69.2%),Rh阴性为40例(30.8%)。
本研究130例孕妇的血清样本中,Rh血型系统不规则抗体为71例(54.6%),MNSs血型系统为28例(21.5%),P血型系统为3例(2.3%),Lewis血型系统为14例(10.8%)。此外,抗-HI为4例(3.1%),未能确定抗体特异性为10例(7.7%)。本研究130例孕妇血清样本不规则抗体的血型系统分布,见表1。
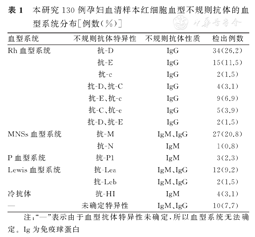
本研究130例孕妇血清样本红细胞血型不规则抗体的血型系统分布[例数(%)]
本研究130例孕妇血清样本红细胞血型不规则抗体的血型系统分布[例数(%)]
| 血型系统 | 不规则抗体特异性 | 不规则抗体性质 | 检出例数 |
|---|---|---|---|
| Rh血型系统 | 抗-D | IgG | 34(26.2) |
| 抗-E | IgG | 15(11.5) | |
| 抗-c | IgG | 2(1.5) | |
| 抗-D、抗-C | IgG | 4(3.1) | |
| 抗-E、抗-c | IgG | 9(6.9) | |
| 抗-C、抗-e | IgG | 5(3.9) | |
| 抗-D、抗-E | IgG | 2(1.5) | |
| MNSs血型系统 | 抗-M | IgM、IgG | 27(20.8) |
| 抗-N | IgM | 1(0.8) | |
| P血型系统 | 抗-P1 | IgM | 3(2.3) |
| Lewis血型系统 | 抗-Lea | IgM、IgG | 12(9.2) |
| 抗-Leb | IgM、IgG | 2(1.5) | |
| 冷抗体 | 抗-HI | IgM | 4(3.1) |
| — | 未确定特异性 | IgM、IgG | 10(7.7) |
注:"—"表示由于血型抗体特异性未确定,所以血型系统无法确定。Ig为免疫球蛋白
本研究71例检出Rh血型系统不规则抗体孕妇的抗体效价检测结果显示,抗体效价为2的检出率最高,为26.8%(19/71)。抗体效价系512的孕妇为1例,其Rh血型为Rh阴性,既往有RhD阳性红细胞制品输血史。本研究71例检出Rh血型系统不规则抗体孕妇的抗体效价分布,见表2。
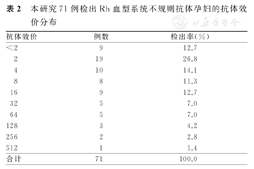
本研究71例检出Rh血型系统不规则抗体孕妇的抗体效价分布
本研究71例检出Rh血型系统不规则抗体孕妇的抗体效价分布
| 抗体效价 | 例数 | 检出率(%) |
|---|---|---|
| <2 | 9 | 12.7 |
| 2 | 19 | 26.8 |
| 4 | 10 | 14.1 |
| 8 | 8 | 11.3 |
| 16 | 9 | 12.7 |
| 32 | 5 | 7.0 |
| 64 | 5 | 7.0 |
| 128 | 3 | 4.2 |
| 256 | 2 | 2.8 |
| 512 | 1 | 1.4 |
| 合计 | 71 | 100.0 |
随着计划生育政策的调整,我国目前已进入全面两孩时代,母婴之间红细胞血型不规则抗体引起的免疫反应发生率随之增高。妊娠是红细胞血型不规则抗体产生的主要原因之一,母婴血型不合导致的HDN应当引起产科及新生儿科医师的重视。HDN通常特指母婴血型不合引起的胎儿或者新生儿免疫性溶血性疾病。由于母亲体内存在与胎儿血型不相容的IgG型血型抗体,抗体通过胎盘进入胎儿血液循环,产生抗原-抗体反应,导致胎儿溶血,严重者可引起流产、早产、死胎,以及新生儿发生溶血性贫血、水肿及核黄疸等。引起HDN的抗体主要来源于ABO、Rh、Kell、Duffy、Kidd、MNSs及Lewis等血型系统[4,5]。
不同血型抗原对应的不规则抗体的产生频率,主要取决于其抗原的免疫原性及表达量。在妊娠过程中,由于胎儿与母体之间存在着复杂的免疫反应和胎盘屏障的透通性,IgG类型的不规则抗体可通过胎盘进入胎儿体内,引起HDN[4]。因此,红细胞血型不规则抗体检测对降低HDN风险尤为重要。本研究130例红细胞血型不规则抗体初筛结果呈阳性的孕妇中,检出Rh血型系统不规则抗体最多,总计71例,占54.6%,其中抗-D占26.2%(34/130),抗-E占11.5%(15/130),该结果与抗-D、抗-E的免疫原性强相对应。检出MNSs血型系统不规则抗体28例,占21.5%,其中27例为抗-M,其中大部分属于天然抗体。此外,检出Lewis血型系统不规则抗体14例,占10.8%,以IgM抗体为主,部分合并IgG抗体。通常Lewis血型系统不规则抗体不会引起严重的HDN[6]。本研究结果提示,孕妇检出的红细胞血型不规则抗体涉及多个血型系统,因此应提高实验室血型系统不规则抗体的检出能力,避免漏检。
Rh血型系统包括D、C、E、c、e 5种抗原,其对应的Rh血型系统不规则抗体是目前临床最易检出的不规则抗体,通常存在于有输血史或妊娠史的患者血清样本中。其中,以抗-D引起的Rh-HDN相对多见,亦可见抗-E、-C、-c及联合抗体引起HDN的报道[7]。本研究71例检出Rh血型系统不规则抗体的孕妇中,抗体效价为2的检出率最高(26.8%,19/71),而抗体效价最高值为512,该孕妇曾于多年前接受过RhD阳性红细胞制品输注。目前,对于抗体效价的检测结果并没有确定的标准,通常认为孕妇Rh血型系统不规则抗体效价越高,其分娩新生儿的HDN发病风险越大,病情越严重。文献报道,若Rh血型系统不规则抗体效价≥16时,对HDN的临床指导意义较大,但是目前该标准未获得临床共识[8]。因此,对于Rh血型系统不规则抗体,只要孕妇体内捡出此类抗体,无论其效价高低,临床上均应密切关注HDN的发生风险。若孕妇Rh血型系统不规则抗体效价随孕周的增加而升高,临床上应予高度重视,加强对孕妇的监测,对产后新生儿应立即进行HDN血清学相关检测,病情严重者应及早进行换血治疗[9]。
针对红细胞血型不规则抗体筛查阳性的孕妇,首先应通过不规则抗体鉴定试验确定不规则抗体的特异性,其次需要确认被检者相应抗原是否为阴性。检测孕妇红细胞血型不规则抗体效价是预测其新生儿HDN严重程度的最常用方法,当检出IgG抗体时,应进行抗体效价的测定并定期复查,建议妊娠28周之前,每4周检测1次,妊娠28周至分娩,每2周检测1次,进行不规则抗体鉴定及抗体效价分析。分娩后,留取新生儿血液标本或脐带血进行HDN相关检测[10]。
通过对孕妇进行红细胞血型不规则抗体的筛查及鉴定试验,能够发现具有临床意义的不规则抗体,进而选择相配合的血液输注,确保输血安全,及早评估、预测HDN的发生,采取措施进行预防,有效缓解症状。因此,笔者建议将孕妇不规则抗体筛查作为产前检查的常规检测项目。
所有作者均声明不存在利益冲突



























