
牙周炎可致牙周组织破坏、牙齿松动和脱落,严重影响患者生活质量。牙周再生手术是修复牙周组织缺损的重要治疗手段,也是目前牙周临床和基础研究的重点。全面了解影响牙周再生手术疗效的相关因素能增强临床医师的牙周治疗理念,增加治疗效果的可预期性,提升临床综合诊疗水平。本文阐述牙周再生的基本原则和牙周创面愈合的要点,从患者因素、局部因素、手术因素以及再生材料选择方面全方位剖析影响牙周再生手术临床效果的各项要素,以期对临床医师有所帮助。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,2023年从第1期至第8期共刊发11篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获5分。
由于可导致牙周软硬组织严重破坏和牙齿松动,重度牙周炎若不及时控制则可进一步发展至Ⅳ期牙周炎[1],最终导致牙齿脱落。随着我国经济发展和人民生活水平的不断提高,人民对口腔治疗的需求已从简单的拔补镶,进阶到追求功能、美观和牙周健康。因此,口腔医师,特别是从事牙周专科相关治疗领域的临床医师,需要对牙周再生手术有透彻的了解,而不是仅止步于掌握牙周基础治疗手段。随着对创伤愈合和牙周再生手术生物学原理的深入探索,基础研究、长期临床研究和系统综述已证实各种牙周重建或再生手术能取得一定的临床疗效[2, 3, 4],包括牙周翻瓣清创术、牙周植骨术(bone grafting)、引导性组织再生术(guided-tissue regeneration,GTR)和生长因子植入[如釉基质蛋白衍生物(enamel matrix proteins,EMD)、血小板衍生生长因子-BB(platelet-derived growth factor-BB,PDGF-BB)等],或几种技术的联合应用。通常牙周再生手术可获得以下临床疗效:改善牙周重度破坏患牙的牙周附着水平(获得新附着)、降低患牙探诊深度(probing depth,PD)、恢复或提升牙槽骨高度[5]。
面对日新月异的各类再生材料和新技术,只有全面了解牙周再生手术的各项影响要素,才能因势利导地针对不同牙周状况作出正确的治疗决策。本文结合生物学原理、循证医学证据和临床治疗经验,全面剖析影响牙周再生的各项要素,并从牙周再生手术原则、患者相关因素、局部相关因素、手术相关因素以及再生材料选择等方面逐一分析,以期对临床医师有所帮助。
牙周组织包含牙龈上皮、牙龈结缔组织、牙周膜、牙骨质和牙槽骨5种组分,相比其他口腔软硬组织,牙周组织的创伤愈合过程更复杂。牙周再生中新附着形成隐含的组织学基础包括:根面上新生的牙骨质,新生牙槽骨、牙龈以及最关键的功能性牙周膜(牙周韧带)穿通连接于牙骨质和牙槽骨之间。若想获得理想的牙周再生效果,则必须深入理解牙周组织愈合的机制。绝大多数情况下,通过牙周再生手术实现组织学上的完全再生是非常困难的。现有的组织学研究结果提示,仅在手术治疗的牙根根方位置可能形成新附着,而在靠近骨缺损的最冠方区域,牙周修复组织一般形成上皮性结合[6, 7]。深入理解牙周组织愈合机制,全方位优化再生手术技术,才能获得更多的牙周再生组织,避免形成过多的上皮性结合,进而影响再生手术的长期疗效。需要指出的是,临床治疗中较难通过组织学检测评价牙周再生手术效果,通常以临床附着水平(clinical attachment level,CAL)的改善、PD的减少和影像学上骨高度和骨密度的增加衡量牙周再生手术的临床疗效。
多项动物和组织学研究结果证实,健康牙周膜组织和(或)细胞的保存、伤口和血凝块的稳定、再生空间的维持、创面组织的封闭(一期愈合)是实现以新附着形成为主的理想牙周再生临床疗效的基本生物学原则[8]。基于以上创伤愈合的要素并结合临床手术的特点,Wang和Boyapati[9]提出获得良好骨再生的4项基本手术原则(PASS原则):初期创面关闭(primary wound closure)——确保下方伤口愈合过程不受外界刺激和干扰;充足的血供(angiogenesis)——提供新鲜血液养分和未分化的间充质干细胞,牙周再生中牙周膜干细胞和骨髓间充质干细胞均是关键的再生前体细胞;空间的支撑和(或)创造(space maintenance/creation)——去除病变组织,保留健康牙周膜,并预留足够空间以便新生牙周组织能长入缺损空间内形成更多的新附着,避免出现大量的上皮性结合;创面的稳定(stability of wound)——无张力的创面愈合可诱导血凝块形成,并确保愈合过程中血凝块的稳定,以促进牙周再生。PASS原则对牙周再生手术也具有指导作用和启示意义。
S3级牙周临床治疗指南中明确提出行牙周再生手术的条件:①对于完善的牙周基础治疗后仍存在PD>5 mm且骨内缺损(骨下袋深度)≥3 mm的牙位,推荐施行牙周再生手术;②推荐下颌Ⅱ度和上颌颊侧Ⅱ度根分叉病变行牙周再生手术[10]。若患者符合以上牙周再生手术条件,则医师应进一步从患者相关因素、局部相关因素、再生材料的选择和手术相关因素方面深入评估(表1)。在患者充分了解病情并共同参与讨论的前提下,制订最恰当的再生治疗方案。

牙周再生手术临床疗效影响因素的分析步骤
牙周再生手术临床疗效影响因素的分析步骤
| 步骤 | 影响因素 | 分析内容 |
|---|---|---|
| 第一步 | 患者相关因素 | 全口菌斑指数:<20% 全口出血指数:<20% 吸烟情况:<10支/d 糖尿病:控制稳定 |
| 第二步 | 局部相关因素 | 骨缺损形态:1壁、2壁、3壁、环形缺损 牙齿松动度:Ⅰ、Ⅱ、Ⅲ度 牙髓活力:正常或死髓 角化龈:宽度、厚度 |
| 第三步 | 再生材料的选择 | 骨替代材料:自体骨、脱钙冻干骨、异种小牛骨基质 屏障膜:可吸收胶原膜 生长因子:重组人血小板衍生生长因子-BB |
| 第四步 | 手术相关因素 | 切口设计:改良龈乳头保护技术、简化龈乳头保护瓣 翻瓣清创:微创手术技术、改良微创手术技术、延伸翻瓣 复位缝合:无张力复位、一期愈合、改良内褥式缝合 术后护理:防出血、抗感染、稳定创面 |
与其他所有手术一样,患者相关的影响因素对牙周再生手术的决策和预后疗效也有不可低估的影响,术前应仔细评估并积极控制风险因素。多项系统综述和荟萃分析显示,牙周炎症与菌斑的控制、患者依从性、吸烟情况、糖尿病以及全身状况等均可影响牙周再生手术的临床疗效[5,11, 12]。
根据S3级牙周临床治疗指南[10],仅在完善第一步控制风险因素和第二步控制牙周炎症,并且患者可进行良好的自我菌斑控制且依从性良好的前提下,才能进入第三步——牙周手术治疗阶段。具体而言,牙周再生手术前的评估阶段全口菌斑指数(full-mouth plaque score,FMPS)和全口牙龈出血指数(full-mouth bleeding score,FMBS)均必须<20%。多项临床研究提示菌斑和牙龈出血控制得越好,再生手术后CAL增加量越多[2,13]。此外,患者良好的依从性,能主动积极配合治疗,加强自我菌斑控制和维护,也是实施牙周再生手术的重要先决条件。对于计划进行牙周再生手术的位点,若仍有探诊出血或牙龈炎症,则可在术前尝试于局部麻醉下再行局部龈下刮治和温和的根面平整(避免过度去除健康牙周组织),必要时也可联合使用局部抗菌药物(如盐酸米诺环素、氯己定等)[14]。
2018牙周病和植体周病新分类中明确指出,吸烟和糖尿病是牙周病的风险因素[15]。相比非吸烟者,吸烟者口内的创伤愈合能力显著下降,牙龈组织的血供也减少,更易出现伤口开裂[16]。一项临床研究显示,吸烟者(特别是每天吸烟超过10支者)牙周再生术后CAL增加量远低于非吸烟者[(2.1±1.2)mm对比(5.2±1.9)mm][17]。因此,术前应建议患者尽可能戒烟,若无法彻底戒除,则需降低每日吸烟量至10支以下,否则手术失败风险将急剧提升。当血糖控制不佳时,患者自身的免疫能力和创伤愈合能力大幅降低。因此,对于需行牙周再生手术的糖尿病患者,应首先将糖化血红蛋白水平控制稳定(HbA1C<7%)。
此外,年龄、性别、生活和精神压力以及是否存在基础疾病和相关用药史也是可能影响牙周再生手术疗效的因素。建议将这些信息纳入牙周再生手术的术前资料收集。总之,良好的菌斑和炎症控制,无吸烟史、糖尿病等不良局部和全身因素是牙周再生手术获得良好疗效的先决条件。
1.骨缺损的形态:骨缺损形态是影响牙周再生手术疗效的重要因素,其不但影响牙周再生手术的材料和术式选择,更是决定再生或重建性手术疗效的关键[18]。如前所述,骨缺损深度≥3 mm是牙周再生手术适应证。
2021年发表的关于骨缺损形态对牙周再生手术临床疗效影响的系统综述指出,相比初始骨缺损深度≤4 mm的位点,初始骨缺损深度>4 mm的位点影像学骨增量平均多0.75 mm(95%CI 0.38~1.12 mm),且骨下袋越深术后获得的再生效果越好[19]。另外一项多中心随机对照研究显示,无论骨下袋深浅,GTR比单纯翻瓣清创能多获得1 mm以上的CAL增加量[20]。有趣的是,1年随访时虽然深骨下袋的CAL增加量多于浅骨下袋,但再生治疗组中不同深度骨下袋的CAL增加量百分比(术后1年CAL增加量÷基线CAL×100%)比较显示,两者结果均为75%左右,差异并无统计学意义。与此同时,骨下袋的宽度越宽(>3 mm),开口越大,其获得再生的能力越低,临床研究显示其骨再生和CAL的增加量也越少。骨缺损顶部至底部连线与牙长轴形成的夹角——缺损角度也是影响再生效果的因素,已有研究显示,较窄的骨缺损(缺损角度<22°)相比较宽(缺损角度>37°)的骨缺损,CAL增加量平均多1.2 mm,且取得3 mm以上CAL增加量的概率可提高2.5倍[21]。因此,应在条件允许的情况下尽可能进行牙周再生手术治疗,越是窄而深(缺损角度<37°,深度>3 mm)的骨缺损,牙周再生手术疗效的可预期性越好;相对而言,宽而浅的骨下袋所能获得的牙周再生量较有限。
剩余骨壁数量可决定骨缺损是否为包容性缺损。相比1壁骨缺损,3壁及2壁骨缺损一方面能更好地维持再生材料的稳定,另一方面成骨细胞和血供来源也更丰富,因此牙周再生能力也显著增加。剩余骨壁数量可直接影响牙周再生手术术式和再生材料的选择[22]。需要特别指出的是,随着牙周微创再生手术技术的进展和各种再生材料的联合应用,即使1壁骨缺损也能通过合适的牙周再生技术获得较好的临床疗效,但相关的技术敏感性和手术难度也较大。
2.牙齿松动度:牙齿松动度也是影响牙周再生疗效的重要因素,特别是当松动度≥Ⅱ度(水平松动度>1 mm,或伴近远中向的活动度)时,手术创面的稳定性大大降低,再生材料在愈合过程也可能因受 力干扰而漏出。
力干扰而漏出。
因此,当牙齿松动度<Ⅱ度且无咬合创伤时,牙周再生术前常无须特别处理。但若患牙松动度≥Ⅱ度,则应先排除咬合创伤,必要时进行咬合调整。虽然缺乏严格的随机对照研究验证,但于牙周再生手术前行临时性或半永久性牙周夹板固定松动度≥Ⅱ度的患牙已成为共识[23]。需要注意,固定松动牙的装置可影响患者的菌斑控制,且常有一定异物感,必须提前对患者进行良好的宣教,并指导其使用牙间隙刷清洁邻面。术后3~6个月若获得良好的牙周再生,则可考虑拆除临时性牙周夹板。
3.牙髓活力:牙髓活力状况也可影响牙周再生手术的临床疗效,特别是对于牙周破坏已接近根尖(骨袋底至根尖<3 mm)的患者,应首先评估牙髓活力状况。若存在牙体病变或牙髓活力异常,则应先行牙体或根管治疗。已有研究显示,完善的根管治疗并不对牙周再生手术疗效造成任何负面影响[24]。对于存在根尖周病变且伴牙周破坏的患牙,建议完善牙周基础治疗和根管治疗后3个月,再评估是否需行牙周再生或重建手术。这样可观察根管治疗后的恢复情况,使因牙髓炎症导致牙周破坏的组织得以自愈,简化甚至避免额外的手术治疗。
4.角化龈宽度和厚度:随着牙周治疗理念的全面建立以及对创伤愈合机制认识的不断深入,临床医师意识到硬组织再生建立于软组织良好的封闭基础上[25]。角化龈的宽度和厚度也可能是影响牙周再生手术疗效的关键因素,患者角化龈宽度>2 mm且为厚牙周表型时,有利于施行牙周再生手术治疗[26]。一方面有利于更好地封闭创面,抵抗愈合过程中菌斑等不良刺激影响下方的再生材料;另一方面,较厚的牙龈组织也能降低缝合过程中撕裂的风险,便于手术操作。因此,对于部分软硬组织同时严重缺损的病例,有时需先行软组织移植以增宽增厚角化龈,或同期进行软硬组织增量,如采用结缔组织移植物墙技术等方法[27]。
常用的牙周再生生物材料包括:骨移植材料、生物屏障膜和各类生长因子。根据美国牙周病学协会推荐的牙周再生共识,现今循证医学证据最充分、应用最广泛的植骨移植材料为自体骨、脱钙冻干骨、异种小牛骨基质[25,28]。此外,也有大量长期临床及基础研究证实可吸收屏障膜、EMD及PDGF-BB的可靠性[29, 30, 31, 32]。根据不同的骨缺损类型和残余骨壁数量,选择不同的牙周再生材料:3壁骨袋、环形缺损且缺损宽度<2 mm时单独使用骨移植材料、生物屏障膜或各类生长因子;3壁骨缺损、环形骨缺损且缺损宽度≥3 mm,或2壁骨缺损时需采用移植骨材料+屏障膜或移植骨材料+生长因子;1壁骨袋应联合使用各种材料的手术技术,并尽可能混合自体骨等含自体细胞的材料以提供更多的再生细胞[22]。
3壁或2壁骨缺损再生各类骨移植材料的手术疗效可预期性较好,1壁骨缺损仍是目前较难的临床挑战,而对于水平型骨缺损(0壁),现有的再生材料和技术仍无法取得理想的再生效果,因此不适合行牙周再生手术[22]。牙周再生手术中材料的成本常占据较大比例,事实上并没有最好的牙周再生材料,作为临床医师应仔细了解各种材料和生物因子的不同特性,并根据患者的经济能力和临床状况进行全面的医患沟通后,才能做出最合适的抉择。
基于对牙周再生手术原则的理解,牙周再生手术向更微创且精细的方向不断发展。不但需清创以彻底去除病变和感染组织,更重要的是保存健康的牙龈及龈乳头,并分辨根面上健康的牙周膜,将其保留作为再生的种子细胞[33]。
若想牙周再生手术取得更好的疗效,还应选用合适的微创手术器械、头戴式或眼镜式放大镜或显微镜以及更精细的缝线。此外,就具体手术而言,应因时制宜地把握以下四点:切口设计、翻瓣清创、复位缝合和术后护理。手术技术是影响牙周再生疗效的重中之重,也是临床医师可通过学习和实践提高并掌握的内容。再次强调,手术相关的改良和设计均必须基于牙周再生创伤愈合原则。
1.切口设计:牙周再生手术的切口在龈乳头区需根据邻间宽度(龈乳头基底部宽度)决定采用何种龈乳头保护切口,建议使用显微手术刀片做切口。龈乳头宽度>2 mm、基底较宽(如上前牙区)时,可采用改良龈乳头保护技术(modified papilla preservation technique,MPPT)[34](图1A,B)。具体方法:于唇颊侧龈乳头基底部做水平切口,将整个龈乳头推至舌腭侧,而颊侧瓣可进行彻底松弛后冠向复位。在邻间骨下缺损区植入再生材料后采用水平内褥式缝合减张并复位龈乳头覆盖于骨缺损区上方,使创面一期愈合,稳定下方血凝块和再生材料。但龈乳头宽度≤2 mm、基底较窄(下前牙区及磨牙区常见)时,若仍采用MPPT则可大大增加龈乳头坏死的概率,此时建议采用简化龈乳头保护瓣(simplified papilla preservation flap,SPPF)[35](图1C,D)。具体方法:于骨缺损对应的龈乳头做一斜行切口,从患牙颊侧轴角位置的龈缘切入,手术刀片始终与牙长轴平行,在颊舌向斜形切开至龈乳头顶点稍偏下方的位置(图1C),从 面观,自患牙颊侧轴角切入至邻牙接近邻面中线的位置(图1D)。以此将整个龈乳头分为包含龈乳头顶部且较大的腭侧瓣和包含较小部分龈乳头的颊侧瓣,采用该方法可较大程度改善龈乳头血供,降低移植材料暴露的概率,从而获得更多的牙周新附着和骨再生。已有文献显示,采用SPPF可获得(4.9±1.8)mm的CAL增加量,67%以上的病例始终维持一期愈合[35]。
面观,自患牙颊侧轴角切入至邻牙接近邻面中线的位置(图1D)。以此将整个龈乳头分为包含龈乳头顶部且较大的腭侧瓣和包含较小部分龈乳头的颊侧瓣,采用该方法可较大程度改善龈乳头血供,降低移植材料暴露的概率,从而获得更多的牙周新附着和骨再生。已有文献显示,采用SPPF可获得(4.9±1.8)mm的CAL增加量,67%以上的病例始终维持一期愈合[35]。
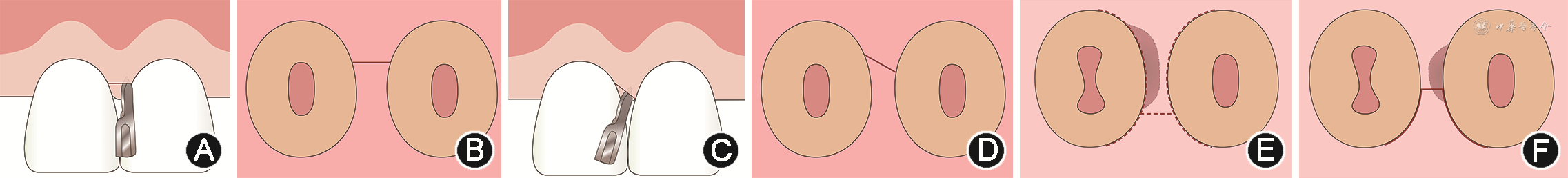
 面观;C:简化龈乳头保护瓣(SPPF)切口(红色线段)颊面观;D:SPPF切口(红色线段)
面观;C:简化龈乳头保护瓣(SPPF)切口(红色线段)颊面观;D:SPPF切口(红色线段) 面观;E:微创手术技术翻瓣(红色虚线为切口);F:改良微创手术技术翻瓣(红色曲线为切口)
面观;E:微创手术技术翻瓣(红色虚线为切口);F:改良微创手术技术翻瓣(红色曲线为切口)
 面观;C:简化龈乳头保护瓣(SPPF)切口(红色线段)颊面观;D:SPPF切口(红色线段)
面观;C:简化龈乳头保护瓣(SPPF)切口(红色线段)颊面观;D:SPPF切口(红色线段) 面观;E:微创手术技术翻瓣(红色虚线为切口);F:改良微创手术技术翻瓣(红色曲线为切口)
面观;E:微创手术技术翻瓣(红色虚线为切口);F:改良微创手术技术翻瓣(红色曲线为切口)在颊舌侧龈缘位置,为保留角化组织均采用沟内切口;在无牙区多行牙槽嵴顶的水平延伸切口,仅当角化龈较少,前庭较浅时,建议行稍偏舌腭侧的牙槽嵴顶切口。需确保水平切口位于角化龈上,以获得更好的初期创面封闭效果。如有必要,颊侧瓣的松弛首先推荐采用沟内延伸切口或内水平切口切开骨膜松弛。若张力仍然较大,则可在远中位置附加一道垂直切口进行减张。若仍无法做到无张力的冠向复位完全覆盖移植材料,则建议于术区两端附加两道垂直切口形成梯形瓣进一步松弛。因垂直切口可能导致瘢痕影响美观以及颊侧龈瓣的血供和稳定,临床应尽可能避免使用。选择正确的手术切口能简化手术过程,减少创伤;合适的切口使术区龈乳头、角化龈等软组织得以完整保存,这是牙周再生手术成功的关键要素,也是获得最终良好美学效果的基石,因此针对每例患者必须个性化分析,按照上述原则设计恰当的手术切口并精细地按步实施。
最近也有学者提出各种新的改良手术切口:包括采用改良隧道入路的全乳头保护技术(entire papilla preservation technique)、前庭纵切口入路的改良骨膜下隧道技术(modified vestibular incision subperiosteal tunnel access)和前庭横切口入路的无龈乳头切口手术技术(non-incised papillae surgical approach)等[36, 37, 38],有望进一步优化手术入路,保护龈乳头完整性,减少术后软组织退缩。但目前仍缺乏严格的随机对照研究验证这些新技术的实际临床效果。
2.翻瓣清创:完成切口后,翻瓣的范围和清创的程度可直接决定手术创伤的大小。随着牙周微创手术技术的提出和牙周再生理念的不断完善[39](图1E),主流的再生手术观念是在彻底清除病变组织的前提下,尽可能减小翻瓣范围,尽可能缩短骨面暴露的时间,并最大限度保存健康牙周组织。垂直向上,采用精细的微创骨膜分离器翻全厚瓣暴露至骨缺损底部下方1~2 mm即可,减少非必要的骨面暴露,以保持龈瓣的血供和稳定。水平向上,翻瓣范围也应尽可能小且精细,最好仅限于骨下缺损区累及的牙位及相邻的一个牙位。若为范围较小的3壁或较浅的2壁骨缺损,可采用改良微创手术技术单侧翻瓣入路[40](图1F),保留腭侧龈乳头不翻开,最大程度保存血供和龈乳头高度的稳定。但若骨缺损过深或范围较大(超过3/4的根面),较小的翻瓣无法彻底暴露创面时,则需延伸翻瓣,再向近远中方向多延伸一个牙位。
翻瓣暴露缺损后,建议使用微创刮治器进行细致地清创,彻底去除骨下袋内的病变组织和肉芽;病变的根面上可用超声和手用刮治器进行根面平整并彻底去除残余的龈下菌斑和牙石。但应注意保留骨袋底处附着于根面的健康牙周膜纤维及骨膜,这是牙周再生过程中重要的细胞来源。同时清创过程中必须避免损伤牙槽嵴上的牙周纤维和缺损区对应的龈乳头。清创过程中多用生理盐水冲洗以保持组织的湿润和术野清晰。可选择使用24%乙二胺四乙酸等进行根面处理去除玷污层并开放牙本质小管,但现有研究未能证实此操作能显著提高牙周再生手术的临床疗效[41]。完成以上步骤后将再生材料植入骨缺损中,不建议大量过充填,避免骨替代材料超过剩余骨壁的最高点过多。因为骨壁最高点上方无任何支撑,且过量的材料还可导致伤口张力增大,影响创面的稳定和一期愈合(图2)。
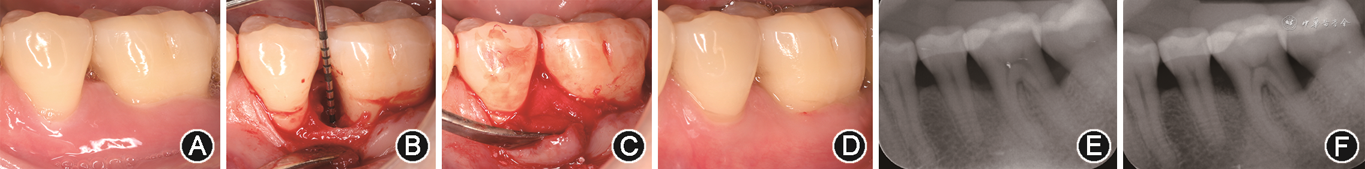

3.复位缝合:缝合目的是获得无张力的一期愈合,完全封闭创口才能使下方的再生材料和血凝块稳定,避免生物膜或植骨材料暴露,尽可能地实现牙周再生的目标[42]。选择尽可能小的缝针,可避免针眼过大并降低龈瓣意外撕裂的风险。龈乳头区建议使用5-0或6-0号单股不可吸收缝线进行缝合;如有垂直切口则建议使用6-0号单股不可吸收缝线。多股的可吸收缝线常易致菌斑黏附,不利于创面愈合和术后口腔卫生维护。
植入再生材料及龈瓣复位对位后,于龈乳头基底部可先进行内褥式减张缝合,再于上方用圈形间断缝合关闭创面;或采用改良内褥式缝合一次性达到减张和关闭创口的双重目的。颊侧龈瓣较松弛时可附加悬吊缝合将颊侧龈瓣紧贴于根面上。延伸的位置或垂直切口处可采用圈形间断缝合关闭创口。
4.术后护理:术后护理也是牙周再生手术关键的一环,手术完成后才是牙周再生过程的开始。防出血、抗感染、稳定创面是术后护理的关键[43]。为避免术后肿胀及疼痛,及时服用止痛药并于术后早期进行局部冰敷有助于减少术后肿胀和出血。愈合期最初14 d,手术区域不能常规刷牙以免影响创面的稳定,可使用0.12%~0.2%的氯己定每天局部含漱3次。因植入再生材料,术后即刻起,建议连续口服抗生素3~5 d预防感染。术后14 d时创面初步愈合,可拆除缝线。术后1、3、6、12个月定期随访,控制菌斑和局部炎症复发是牙周再生治疗长期成功的基石。此外,还应在术后告知患者整个愈合和组织改建过程可持续半年,愈合早期可能出现牙龈退缩、龈乳头高度降低和少量移植材料漏出。
以上手术要素背后的核心理念是尽可能保留龈乳头,使骨缺损区的空间维持得更好;精细的切口和较小的翻瓣可使血凝块更加稳定;微创的清创方式,可最大程度保存血供和牙周膜,为再生留下种子细胞;合适的缝合达到初期愈合和创面封闭,以及良好的术后护理一步步对应实现再生手术的PASS原则。全身和局部影响因素的控制,选择合适的再生材料以及不断改善再生手术,掌控治疗原则并付诸实践,才能最终使患者获得最大的收益。
谢玉峰, 林智恺, 束蓉. 影响牙周再生手术临床效果的相关因素剖析[J]. 中华口腔医学杂志, 2023, 58(4): 386-392. DOI: 10.3760/cma.j.cn112144-20230207-00031.
上海交通大学医学院附属第九人民医院牙周病科钱洁蕾医师绘制相关模式图
所有作者声明不存在利益冲突
患者男性,35岁,中学教师,临近中考工作压力大,睡眠较少。患者有吸烟习惯10余年,每天吸烟20支,否认糖尿病等系统疾病史,曾于私立牙科诊所“洁牙”。主诉右上后牙咬物不适半年,检查发现14、15之间存在食物嵌塞,15松动度为Ⅱ度,近中PD 9 mm,牙龈退缩1 mm,其余牙位PD3~4 mm。口腔卫生情况不佳,FMPS和FMBS均大于50%。
1.以下哪项不影响该患者的治疗效果()
A.有吸烟习惯
B.诊所洁牙史
C.口腔卫生不佳
D.工作精神压力大
E.不良咬合关系
2.第一步需要进行的治疗是()
A.牙周洁治
B.牙周刮治
C.咬合调整
D.口腔卫生指导,戒烟
E.松牙固定
3.完成基础治疗后,再评估时,15临床检查探诊出血,袋内少量溢脓且PD为8 mm,松动度为Ⅰ度,下一步最合适的治疗是()
A.牙周洁治
B.15局部刮治+上药
C.15拔牙
D.15松牙固定
E.观察随访
4.再次治疗后,根尖片显示15近中角型吸收,骨下袋深度4 mm,此时适合进行()
A.牙周再生手术
B.翻瓣清创术
C.牙龈切除术
D.牙冠延长术
E.膜龈手术
5.如果15近中龈乳头宽度仅为2 mm,此时,龈乳头区最合适的切口为()
A.传统龈乳头保护切口
B.改良龈乳头保护切口
C.简化龈乳头保护切口
D.牙槽嵴顶切口
E.沟内切口



























